胰腺導(dǎo)管腺癌(PDAC)是一種具有高度侵襲性和致死性的惡性腫瘤,其主要特征是能量和間質(zhì)代謝失調(diào)。激活的胰腺星狀細(xì)胞(PSC)可通過代謝串?dāng)_驅(qū)動PDAC的結(jié)締組織形成和腫瘤生長。有鑒于此,國家納米科學(xué)中心聶廣軍研究員和李一葉研究員設(shè)計(jì)了一種程序化納米系統(tǒng),并將其用于雙重糾正PDAC細(xì)胞(過度表達(dá)葡萄糖轉(zhuǎn)運(yùn)蛋白1(GLUT1)和CD71)和PSC的代謝異常,以實(shí)現(xiàn)腫瘤治療。
本文要點(diǎn):
(1)該納米系統(tǒng)由對腫瘤微環(huán)境響應(yīng)、包裹NF-kB抑制劑(TPCA-1)和CD71適配體連接的Glut1 siRNA的脂質(zhì)體組成。研究發(fā)現(xiàn),TPCA-1可使活化的PSC逆轉(zhuǎn)為靜止?fàn)顟B(tài),以阻礙PSC對PDAC細(xì)胞的代謝支持,并促進(jìn)靶向PDAC細(xì)胞的siRNA遞送。
(2)在原位異種移植小鼠模型中,該納米調(diào)節(jié)策略可有效抑制有氧糖酵解和隨后的氧化磷酸化增強(qiáng),以提高抗PDAC的功效。綜上所述,該研究能夠?yàn)閷?shí)現(xiàn)基于不同能量代謝譜的個(gè)性化PDAC治療提供新的見解。
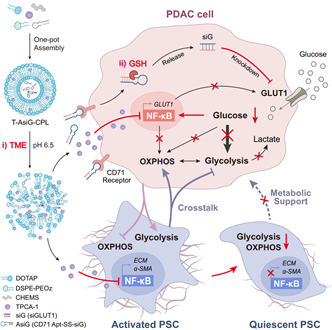
Bowen Wu. et al. Dual rectification of metabolism abnormality in pancreatic cancer by a programmed nanomedicine. Nature Communications. 2024
https://www.nature.com/articles/s41467-024-54963-y



















