雖然靶向表觀遺傳失調(diào)的治療策略能夠用于白血病治療,但表觀遺傳藥物目前仍面臨利用率低、耐藥性和脫靶效應等挑戰(zhàn)。此外,白血病的乏氧微環(huán)境也進一步損害藥物的敏感性。有鑒于此,吉林大學閆飛教授和Yumei Li構(gòu)建了基于MOF的紅細胞仿生納米平臺,其可通過靶向三種表觀遺傳修飾增強抗白血病免疫應答。
本文要點:
(1)實驗利用UiO-66-NH2負載兩種表觀遺傳藥物和富氧紅細胞(red blood cells,RBCs)。MA272@MOF@RBC可抑制乏氧誘導因子(HIF-1α)及其下游癌基因,以增強表觀遺傳藥物的療效。研究發(fā)現(xiàn),這些藥物能夠通過靶向DNA和組蛋白甲基化抑制白血病細胞的生長,并同時增強m6A-RNA甲基化。
(2)實驗結(jié)果表明,MA272@MOF@RBC可通過增加白血病細胞的抗原性激活細胞毒性T細胞和記憶性T細胞。此外,MA272@MOF@RBC也能夠表現(xiàn)出對實體腫瘤的免疫治療作用。綜上所述,該研究構(gòu)建的三重表觀遺傳調(diào)控仿生MOFs在腫瘤免疫治療領域中具有廣闊的臨床應用前景。
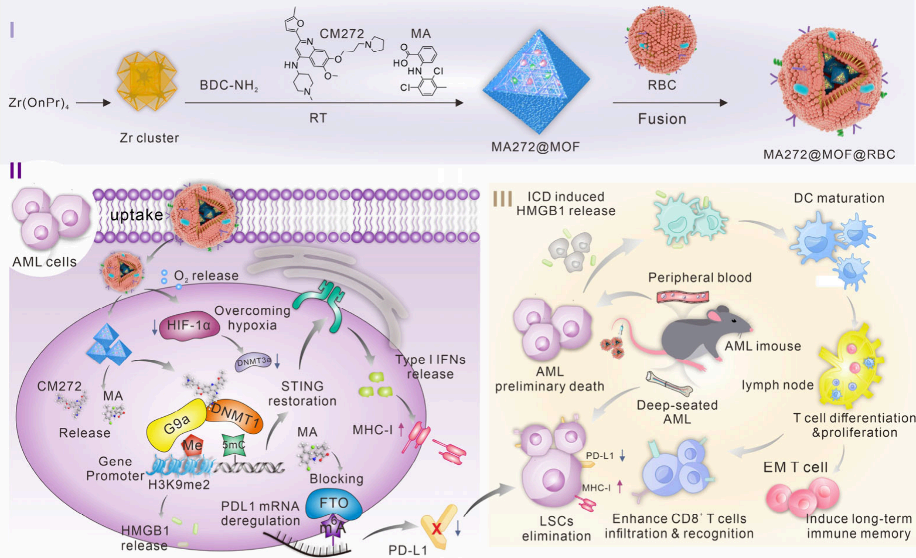
Min Ding. et al. Erythrocyte-Based Biomimetic MOFs as a Triple Epigenetic Regulator for Enhancing Anti-Leukemia Immunity. Nano Letters. 2024
DOI: 10.1021/acs.nanolett.4c04264
https://pubs.acs.org/doi/10.1021/acs.nanolett.4c04264



















