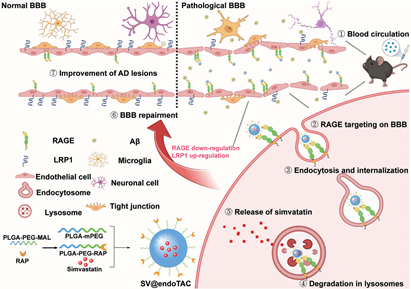
過度上調的晚期糖基化終產物受體(receptor for advanced glycation end products,RAGE,一種重要的病理標志物)會推動阿爾茨海默病(AD)的發生和發展。雖然溶酶體靶向蛋白降解是一種有效的治療方式,但有限的溶酶體分選效率仍會極大地影響靶蛋白的降解。有鑒于此,四川大學高會樂教授開發了一種基于多價受體結合模式的溶酶體-梭狀納米嵌合體(endoTAC),并將其用于增強RAGE降解和實現精準的藥物遞送。
本文要點:
(1)endoTAC可對RAGE表現出高親和力,并且能夠通過與RAGE的多價相互作用促進RAGE降解。研究發現,endoTAC在病變大腦中的積累會發生增加,因此其有望成為一種精準的大腦遞送系統。
(2)體內外實驗結果表明,負載辛伐他汀的SV@endoTAC能夠成功逆轉病理特征。綜上所述,該研究工作將溶酶體靶向嵌合體和有效的藥物遞送系統進行結合的方法能夠為AD治療提供一個新的策略。
Xiaorong Wang. et al. Lysosome-Targeting Protein Degradation Through Endocytosis Pathway Triggered by Polyvalent Nano-Chimera for AD Therapy. Advanced Materials. 2024
DOI: 10.1002/adma.202411061
https://onlinelibrary.wiley.com/doi/10.1002/adma.202411061



















