腫瘤特異性細胞毒性T細胞免疫非常依賴于有效的抗原呈遞和持續的信號轉導。然而,這種免疫反應往往會受到乳腺癌固有的低免疫原性和主要組織相容性復合體I類(MHC-I)表達不足等問題的影響。有鑒于此,廣州醫科大學李仕穎研究員和余睿教授制備了一種能夠增強細胞毒性T細胞應答的嵌合肽工程化聚合前藥(PDPP),其特點是具有較高的載藥量和精準的藥物化學計量比,并且其中的免疫原性細胞死亡(ICD)誘導劑原卟啉IX(PpIX)和表觀遺傳藥物地西他濱(DAC)被縮合為聚合前藥PpIX-DAC。
本文要點:
(1)實驗利用偶聯了程序性死亡配體1(PD-L1)靶向肽序列(CVRARTR)的DSPE-PEG2000-Mal包封PpIX-DAC,以增強乳腺癌靶向藥物遞送。研究發現,PDPP可通過光動力療法(PDT)消融乳腺癌細胞,并同時誘導損傷相關分子模式(DAMPs)的釋放,以增強腫瘤免疫原性。
(2)此外,PDPP也可通過表觀遺傳調節上調MHC-I的表達,協同增強細胞毒性T細胞應答和PD-L1阻斷。實驗結果表明,PDPP能夠誘導強大的抗腫瘤T細胞免疫,有效根除原發性和轉移性乳腺癌。綜上所述,該研究工作能夠為化學計量納米藥物的開發和臨床轉化提供新的借鑒和參考。
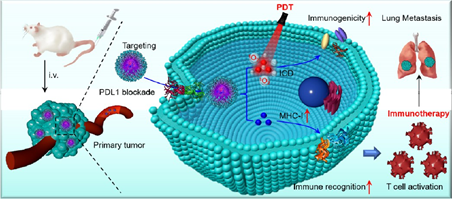
Ying Chen. et al. Chimeric Peptide-Engineered Polyprodrug Enhances Cytotoxic T Cell Response by Inducing Immunogenic Cell Death and Upregulating Major Histocompatibility Complex Class I. ACS Nano. 2025
DOI: 10.1021/acsnano.4c12197
https://pubs.acs.org/doi/10.1021/acsnano.4c12197



















