目前的抗癌治療藥物(包括抗體-藥物偶聯物(ADCs)、寡核苷酸和光敏劑)的腫瘤特異性療效往往會受到細胞穿透性差和藥物遞送效率低等問題的限制。有鑒于此,建國大學Jooho Park和Ji-Hong Lim開發了帶正電、兩親性Ce6偶聯、具有細胞穿透性的抗PD-L1肽納米藥物(CPPD1),其能夠實現增強的細胞和組織穿透。
本文要點:
(1)CPPD1分子是疏水光敏劑和帶強正電荷的程序化細胞死亡配體1(PD-L1)結合細胞穿透肽(CPP)的生物偶聯物,其能夠在水溶液中自組裝成平均尺寸為199 nm的納米顆粒,并且不需要任何載體。研究發現,這些無載體納米顆粒具有穿透癌細胞膜的能力,并且能夠靶向表面表達PD-L1的腫瘤。
(2)CPPD1納米顆粒可有效阻斷程序性細胞死亡-1(PD-1)/PD-L1相互作用,并通過溶酶體降解降低PD-L1的表達。實驗結果表明,CPPD1納米顆粒能夠響應635 nm激光以實現光動力治療(PDT),產生ROS,并誘導多種免疫原性細胞死亡(ICD)。綜上所述,該研究開發的高穿透性CPPD1納米顆粒可以免疫原性地調節CT26癌癥的微環境和治療遠端轉移性腫瘤,有望能夠解決傳統PDT面臨的局限性問題。
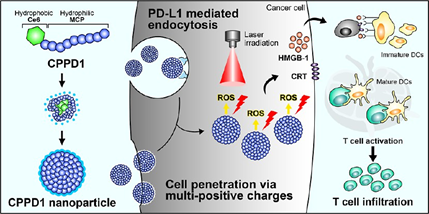
Jun-Hyuck Lee. et al. Cell-Penetrating Peptide Like Anti-Programmed Cell Death-Ligand 1 Peptide Conjugate-Based Self-Assembled Nanoparticles for Immunogenic Photodynamic Therapy. ACS Nano. 2025
DOI: 10.1021/acsnano.4c16128
https://pubs.acs.org/doi/10.1021/acsnano.4c16128



















