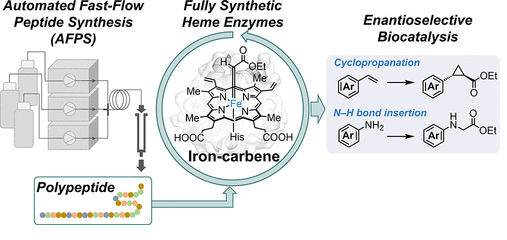
酶催化小分子反應的卓越效率推動了其在有機化學中的廣泛應用。有鑒于此,麻省理工學院Bradley L. Pentelute教授、Stephen L. Buchwald教授等報道采用自動化快速流動固相合成法,能夠不受限制地引入非天然氨基酸的數量和結構,從而獲得具有催化活性的全長酶。
本文要點:
(1)
這項研究展示了鐵依賴性枯草芽孢桿菌肌紅蛋白(BsMb)和抹香鯨肌紅蛋白(SwMb)的全合成過程。合成的酶在卡賓轉移反應中表現出優異的對映選擇性和產率。
(2)
通過使用合成獲得的L-BsMb和D-BsMb突變體,在苯乙烯的環丙烷化反應中,實現了對映選擇性的絕對控制,兩種突變體分別能夠以相同但相反的對映體富集選擇性合成環丙烷產物的不同對映體。
對修飾非天然氨基酸的BsMb突變體進行詳細的構效關系研究,發現了從未被發現的氫鍵相互作用,這種相互作用是苯乙烯環丙烷化反應中對映選擇性的主要動力。作者認為這種方法能夠可靠和快速的生成具有非天然氨基酸的全合成酶,這項工作能夠推動生物催化領域的發展。
參考文獻
Giulio Fittolani, Dennis A. Kutateladze, Andrei Loas, Stephen L. Buchwald*, and Bradley L. Pentelute*, Automated Flow Synthesis of Artificial Heme Enzymes for Enantiodivergent Biocatalysis, J. Am. Chem. Soc. 2025
DOI: 10.1021/jacs.4c13832
https://pubs.acs.org/doi/10.1021/jacs.4c13832


















