MicroRNA(miRNA)會參與結直腸癌的發生和發展。對腫瘤部位的miRNA進行體內成像對于了解其在結直腸癌病理中的作用和治療靶點鑒定至關重要。然而,腫瘤細胞中miRNA的低豐度和正常組織中的非特異性信號泄漏等問題仍會嚴重阻礙對腫瘤部位miRNA的準確成像。有鑒于此,武漢大學袁荃教授、楊雁冰研究員和丁召教授開發了一種多變量門控的催化發夾組裝(CHA)納米傳感器,其能夠在人類結直腸癌組織中對microRNA-21(miR-21)進行特異性放大成像,以揭示與miR-21相關的潛在分子機制。
本文要點:
(1)內源性谷胱甘肽和外源性近紅外多變量門控的設計與CHA探針相結合的策略能夠提高目標miR-21的信號強度,并減少背景干擾。研究發現,該納米傳感器可在體內對miR-21進行特異性放大成像,其信本比是傳統CHA方法的1.6倍。在納米傳感器的輔助下,研究者能夠在臨床手術切除的樣本中成功實現對腫瘤組織和正常組織的初步識別。
(2)實驗結果表明,過表達的miR-21可抑制參與DNA損傷識別和修復的核心錯配修復識別蛋白(人MutS同源蛋白2),從而能夠抑制對結直腸癌的治療效果。綜上所述,該研究提出的探針設計策略將多變量門控激活與信號放大系統相結合,有望為實現精準的miRNA成像和疾病相關的分子機制研究提供一個新的方法。
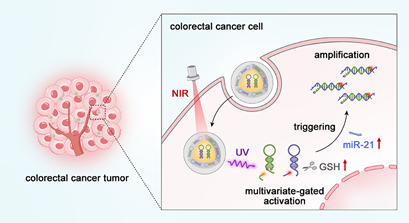
Xiaoming Zhang. et al. Spatially Selective MicroRNA Imaging in Human Colorectal Cancer Tissues Using a Multivariate-Gated Signal Amplification Nanosensor. Journal of the American Chemical Society. 2025
DOI: 10.1021/jacs.4c16001
https://pubs.acs.org/doi/10.1021/jacs.4c16001



















