生理屏障和免疫抑制腫瘤微環境會嚴重影響化療的有效性。癌癥相關成纖維細胞(CAFs)可顯著促進腫瘤細胞外基質(ECM)的重構和抑制免疫反應,是一種重要的治療干預靶點。有鑒于此,華中科技大學甘璐教授和楊祥良教授開發了一種響應腫瘤酸性微環境的遞送系統(DOX@MPs-YM101),該系統將腫瘤細胞源性微粒(MPs)作為化療藥物阿霉素(DOX)和靶向TGF-β和PD-L1的雙特異性抗體YM101的載體,能夠對CAFs和腫瘤細胞進行空間調節,以增強化療的療效。
本文要點:
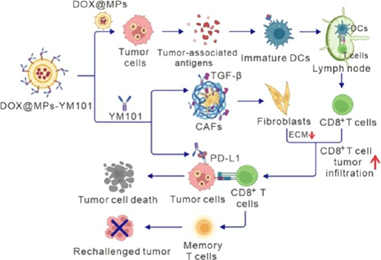
(1)DOX@MPs-YM101可有效靶向腫瘤組織,并通過響應酸性腫瘤微環境釋放DOX@MPs和YM101。YM101能夠重編程CAFs,減少腫瘤ECM,促進DOX@MPs-YM101的腫瘤積聚和深度滲透。研究發現,DOX@MPs能夠被腫瘤細胞高度內化,以觸發免疫原性細胞死亡(ICD),并激活CD8+ T細胞介導的抗腫瘤免疫。
(2)YM101對CAFs的重編程可進一步促進CD8+ T細胞的聚集,減少腫瘤內的免疫抑制細胞的數量。實驗結果表明,YM101能夠有效中和DOX@MPs誘導的腫瘤細胞上的PD-L1,恢復CD8+ T細胞的活性,產生長期的抗腫瘤免疫記憶,防止腫瘤復發。綜上所述,該研究構建的DOX@MPs-YM101在改善癌癥化療的療效等方面具有重要的應用潛力。
Haojie Liu. et al. Spatial Regulation of Cancer-Associated Fibroblasts and Tumor Cells via pH-Responsive Bispecific Antibody Delivery for Enhanced Chemo-Immunotherapy Synergy. ACS Nano. 2025
DOI: 10.1021/acsnano.4c13277
https://pubs.acs.org/doi/10.1021/acsnano.4c13277



















