心肌梗死(MI)嚴重威脅著人類的健康。MI可誘導氧化損傷和炎癥,進而導致心肌死亡、瘢痕形成和心室重構。納米酶具有減輕活性氧(ROS)誘導的損傷和治療心血管疾病的重要潛力。有鑒于此,北京交通大學王海濱教授、中國人民解放軍軍事醫學科學院Gan Chen和周虹教授開發了一種超小的PtIr雙金屬納米酶,并將其用于治療心肌損傷。
本文要點:
(1)PtIr納米酶具有強大的類超氧化物歧化酶和類過氧化氫酶等催化活性,可調節過量ROS轉化為無害產物。研究發現,PtIr納米酶治療可在體外氧化應激條件下降低人心肌細胞AC16細胞的ROS水平和凋亡,并同時增加心肌細胞相關功能基因(包括cTnT、cTnI、Cx43和ACTN2)的表達,維持細胞內線粒體膜電位,增加線粒體活性,保護線粒體結構。在大鼠MI模型中,PtIr納米酶可在給藥后1周有效減輕梗死心臟中的中性粒細胞胞外陷阱的形成、凋亡和炎癥。
(2)在給藥后4周,與PBS組或Ir納米酶治療組相比,PtIr納米酶能夠顯著增強心肌細胞的活性和功能連接性,減少梗死面積和纖維化水平,增加微血管密度。蛋白質組學分析結果顯示,在PtIr納米酶注射組中,與能量代謝、線粒體功能和心肌收縮相關的蛋白表達會發生上調,而脂肪酸β-氧化、檸檬酸循環等與線粒體功能和能量代謝相關的多種通路則會發生富集。綜上所述,該研究構建的PtIr納米酶能夠通過調節線粒體功能和炎癥反應、修復受損心肌以及改善心臟功能等機制重塑梗死微環境,其有望為治療MI提供一種新的策略。
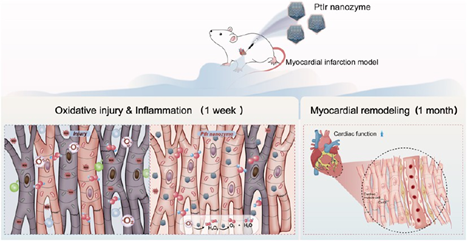
Yuxuan Gong. et al. Ultrasmall PtIr Bimetallic Nanozyme Treats Myocardial Infarction via Ischemic/ Inflammatory Cardiac Microenvironment Remodeling. ACS Nano. 2025
DOI: 10.1021/acsnano.4c14869
https://pubs.acs.org/doi/10.1021/acsnano.4c14869



















