
壽命較短的自由基之間的交叉偶聯(lián)反應(yīng)是有機(jī)化學(xué)領(lǐng)域具有挑戰(zhàn)性的反應(yīng)。
有鑒于此,大阪大學(xué)Takashi Hayashi、Shunsuke Kato等報(bào)道了一種基于硫胺素(Thiamine-)和黃素(Flavin-)依賴酶催化N-雜環(huán)卡賓(NHC)介導(dǎo)的自由基偶聯(lián)反應(yīng)。
本文要點(diǎn):
(1)
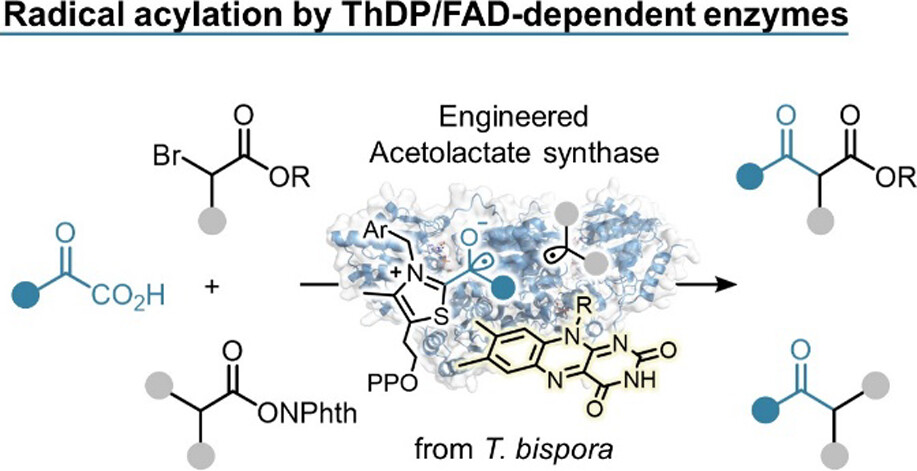
通過(guò)一系列的酶篩選,發(fā)現(xiàn)來(lái)自雙孢嗜熱放線菌(Thermobispora bispora)的乙酰乳酸合酶(TbALS)及其工程化的變體,對(duì)α-溴代羰基化合物的非天然的自由基酰基化反應(yīng)展示了非常好的催化活性。
(2)
值得注意的是,雖然自由基中間體穩(wěn)定性較差,但是TbALS變體對(duì)非芳香族反應(yīng)物具有更高的催化活性。此外,TbALS催化體系可應(yīng)用于利用黃素腺嘌呤二核苷酸(FAD)光氧化還原性質(zhì)的光催化反應(yīng)。在藍(lán)光LED照射下,由N-酰氧基鄰苯二甲酰亞胺生成的非芐基烷基自由基可以高效的轉(zhuǎn)化為二烷基酮。
這些發(fā)現(xiàn)表明硫胺素和黃素依賴酶在壽命較短的自由基選擇性交叉偶聯(lián)反應(yīng)方面的實(shí)用性。
參考文獻(xiàn)
Shunsuke Kato*, Shuto Fujisawa, Yuto Adachi, Mitsuhiro Bandai, Yutaro Mori, Seiji Mori, Tomokazu Shirai, and Takashi Hayashi*, NHC-Mediated Radical Acylation Catalyzed by Thiamine- and Flavin-Dependent Enzymes, J. Am. Chem. Soc. 2025
DOI: 10.1021/jacs.5c04484
https://pubs.acs.org/doi/10.1021/jacs.5c04484


















