放療(RT)可通過引起直接的DNA損傷激活抗腫瘤免疫。然而,由于環(huán)GMP-AMP合成酶(cGAS)對胞質DNA(cDNA)的識別受損,因此放療誘導的免疫應答率較低。同時調控DNA修復和清除系統(tǒng)以增強cDNA的積累是提高免疫應答率的有效方法。有鑒于此,湖南省中醫(yī)藥研究院喻翠云教授和南華大學魏華教授構建了基于二甲雙胍(MET)的多功能納米復合物CS-MET/siTREX1(CSMT),該復合物由作為載體的雙胍修飾的CS(CS-MET)和作為治療基因的3'-5'DNA外切酶TREX1 siRNA(siTREX1)組成,可通過放大初始的DNA損傷信號增強RT誘導的抗腫瘤免疫。
本文要點:
(1)實驗開發(fā)的CSMT可作為特異性DNA損傷放大器,促進cDNA積累,以最大化放射-免疫治療的效果和規(guī)避RT耐藥。研究發(fā)現,CSMT納米復合物不僅能夠通過MET修飾提高基因轉染效率,而且具有協(xié)同治療作用,主要包括MET對DNA修復的抑制以及siTREX1對cDNA清除的弱化,進而能夠實現對Hepa1-6近端/遠端腫瘤模型的抑制效果的最大化,對原發(fā)腫瘤的腫瘤生長抑制(TGI)值高達99.1%,并可通過誘導免疫原性細胞死亡(ICD)顯著抑制遠端腫瘤生長。
(2)此外,該治療策略也能夠促進腫瘤相關中性粒細胞(TAN)的極化,并刺激腫瘤特異性記憶T細胞的產生。綜上所述,該研究開發(fā)的CSMT納米復合物在克服臨床RT耐藥等方面具有廣闊的轉化應用前景。
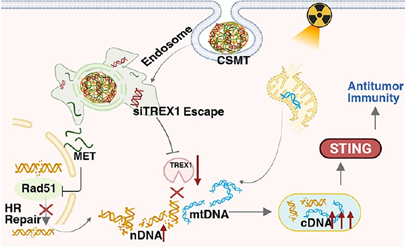
Shuangyan He. et al. A Metformin-Based Multifunctional Nanoplatform as a DNA Damage Amplifier for Maximized Radio-Immunotherapy to Overcome Radiotherapy Resistance. ACS Nano. 2025
DOI: 10.1021/acsnano.4c18627
https://pubs.acs.org/doi/10.1021/acsnano.4c18627



















