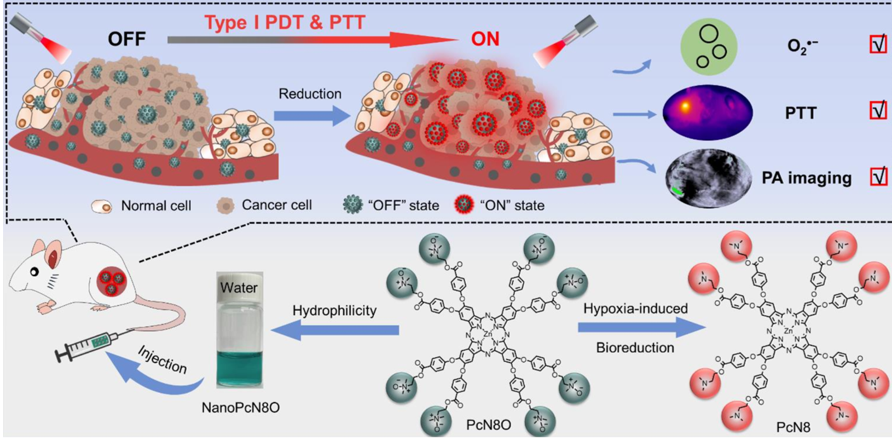
乏氧與腫瘤的增殖、轉移、侵襲和耐藥性密切相關。緩解乏氧對腫瘤治療具有重要影響。具有極低的氧依賴性的I型光敏劑(PSs)是治療乏氧腫瘤的合適候選藥物。然而,缺乏有效的分子設計方法、治療前后PSs對正常組織的光毒性以及親水性差等缺點導致PSs在乏氧腫瘤治療中的應用嚴重受阻。如何開發具有良好的耐乏氧性和低副作用的親水性PS成為了一項亟待解決的難題。有鑒于此,福州大學李興淑教授和梨花女子大學Juyoung Yoon開發了一種基于親水性酞菁衍生物(PcN8O)的自組裝納米治療制劑(NanoPcN8O),其是一種具有乏氧響應性的可生物還原光學診療制劑,能夠實現可激活的光聲成像和腫瘤治療。
本文要點:
(1)多種腫瘤的乏氧區域都具有很強的還原能力。只有這種乏氧條件下,具有多個N-氧化物基團的NanoPcN8O才會被生物還原生成具有豐富的富電子叔胺基團的產物NanoPcN8,以開啟I型光動力和光熱效應,促進I型活性氧(ROS)和熱的產生。
(2)在臨床前模型中,NanoPcN8O能夠實現乏氧誘導的選擇性PA成像。實驗結果表明,乏氧誘導的可切換I型光動力治療(PDT)和光熱治療(PTT)策略具有顯著的光學治療效果和較高的生物安全性。綜上所述,該研究構建的NanoPcN8O有望為克服光學治療中的乏氧耐藥性提供一種新的策略。
Yuan-Yuan Zhao. et al. A Hypoxia-Triggered Bioreduction of Hydrophilic Type I Photosensitizer for Switchable In Vivo Photoacoustic Imaging and High-Specificity Cancer Phototherapy. Angewandte Chemie International Edition. 2025
DOI: 10.1002/anie.202506412
https://onlinelibrary.wiley.com/doi/10.1002/anie.202506412



















