靶向蛋白降解(TPD)能夠根除與發病相關的蛋白(特別是那些曾經被認為是不可成藥的蛋白質組),是一種極具發展前景的治療范式。三磷酸腺苷(ATP)是細胞活動的主要能量來源,而溶酶體則是重要的ATP儲存位點。有鑒于此,復旦大學劉寶紅教授構建了基于雙功能四面體DNA框架的溶酶體靶向嵌合體(TDF-LYTACs),以闡明通過溶酶體途徑降解細胞外蛋白質與細胞內ATP水平波動之間的關系。
本文要點:
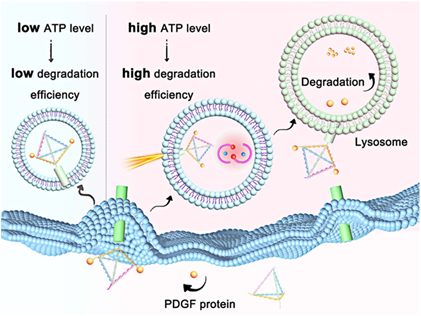
(1)該研究以血小板衍生的生長因子(PDGF,一種癌癥侵襲和轉移的驅動因子)作為感興趣的蛋白質。為了實現多功能性,研究者采用了由PDGF適配體、人類無嘌呤/無嘧啶核酸內切酶1(APE1)觸發的ATP探針和細胞表面溶酶體穿梭受體(IGFIIR)配體組成的四面體DNA框架。
(2)TDF-LYTACs能夠高效、快速地將PDGF蛋白運送到溶酶體,進而通過溶酶體途徑降解PDGF蛋白,并且可以同步可視化細胞內的ATP水平。實驗結果表明,PDGF的降解效率與隨時間變化的細胞內ATP水平之間存在顯著的相關性;即ATP水平越高,降解效率越高,反之亦然。綜上所述,該研究構建的TDF-LYTACs能夠為降解多功能細胞外蛋白提供一個新的有效工具。
Yujun Ning. et al. DNA Framework-Based Lysosome-Targeting Chimeras: Intracellular ATP-Facilitated Extracellular Protein Degradation. ACS Nano. 2025
DOI: 10.1021/acsnano.5c00745
https://pubs.acs.org/doi/10.1021/acsnano.5c00745



















